Топлинният капацитет на газ е количеството енергия, което тялото абсорбира, когато се нагрее с един градус. Нека анализираме основните характеристики на това физическо количество.

Определения
Специфичната топлина на газ е единицата маса на определено вещество. Неговите мерни единици са J/(kg·K). Количеството топлина, което се абсорбира от тялото в процеса на промяна на агрегатното му състояние, е свързано не само с началното и крайното състояние, но и с метода на преход.

Отдел
Топлинният капацитет на газовете се разделя на стойността, определена при постоянен обем (Cv), постоянно налягане (Cр).
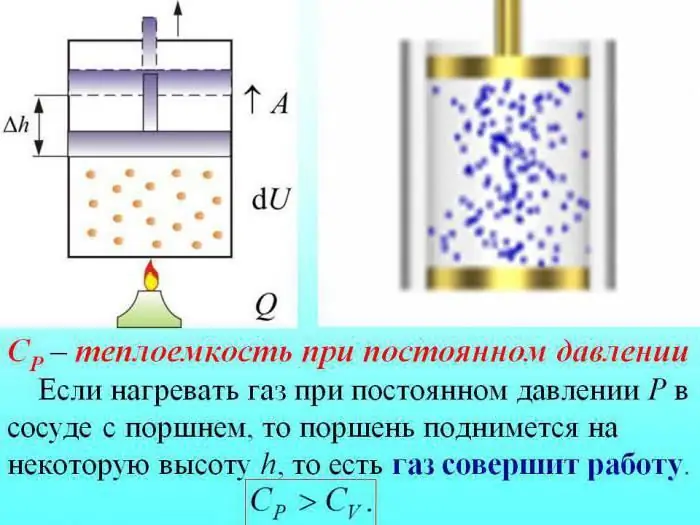
В случай на нагряване без промяна на налягането, част от топлината се изразходва, за да се произведе работата по разширяването на газа, а част от енергията се изразходва за увеличаване на вътрешната енергия.
Топлинният капацитет на газовете при постоянно налягане се определя от количеството топлина, което се изразходва за увеличаване на вътрешната енергия.
Състояние на газа: характеристики, описание
Топлинният капацитет на идеален газ се определя, като се вземе предвид фактът, че Сp-Сv=R. Последната величина се нарича универсална газова константа. Стойността му съответства на 8,314 J/(mol K).
При извършване на теоретични изчисления на топлинния капацитет, например, описване на връзката с температурата, не е достатъчно да използвате само термодинамични методи, важно е да се въоръжите с елементи на статичната физика.
Топлинният капацитет на газовете включва изчисляване на средната стойност на енергията на транслационното движение на някои молекули. Такова движение се обобщава от ротационното и транслационното движение на молекулата, както и от вътрешните вибрации на атомите.
В статичната физика има информация, че за всяка степен на свобода на въртеливо и транслационно движение има количество за газ, което е равно на половината от универсалната газова константа.

Интересни факти
Приема се, че частица от едноатомен газ има три транслационни степени на свобода, така че специфичната топлина на газа има три транслационни, две ротационни и една вибрационна степени на свобода. Законът за равномерното им разпределение води до приравняване на специфичната топлина при постоянен обем на R.
По време на експериментите беше установено, че топлинният капацитет на двуатомен газ съответства на стойността R. Такова несъответствие между теорията и практиката се обяснява с факта, че топлинният капацитет на идеалния газ е свързан с квантовата ефекти, следователно, когато се правят изчисления, е важно да се използва статистика, базирана на квантмеханика.
Въз основа на основите на квантовата механика, всяка система от частици, които осцилират или се въртят, включително газовите молекули, има само някои дискретни стойности на енергия.
Ако енергията на топлинното движение в системата не е достатъчна за възбуждане на трептения с определена честота, такива движения не допринасят за общия топлинен капацитет на системата.
В резултат на това определена степен на свобода става "замразена", невъзможно е да се приложи законът за равноподеляне към нея.
Топлинният капацитет на газовете е важна характеристика на състоянието, от което зависи функционирането на цялата термодинамична система.
Температурата, при която законът за равноразпределението може да бъде приложен към вибрационната или ротационната степен на свобода, се характеризира с квантовата теория, свързва константата на Планк с константата на Болцман.

Диатомни газове
Разликите между нивата на ротационна енергия на такива газове са малък брой градуси. Изключение прави водородът, при който стойността на температурата се определя от стотици градуси.
Ето защо топлинният капацитет на газ при постоянно налягане е трудно да се опише със закона за равномерно разпределение. В квантовата статистика при определяне на топлинния капацитет се взема предвид, че нейната вибрационна част в случай на понижаване на температурата бързо намалява и достига нула.
Този феномен обяснява факта, че при стайна температура практически няма вибрационна част от топлинния капацитет, т.к.двуатомен газ, той съответства на константата R.
Топлинният капацитет на газ при постоянен обем в случай на нискотемпературни индикатори се определя с помощта на квантова статистика. Съществува принципът на Нернст, който се нарича третият закон на термодинамиката. Въз основа на неговата формулировка, моларният топлинен капацитет на газа ще намалява с понижаване на температурата, стремейки се към нула.

Характеристики на твърдите вещества
Ако топлинният капацитет на смес от газове може да се обясни с помощта на квантова статистика, тогава за твърдо агрегатно състояние термичното движение се характеризира с леки флуктуации на частиците близо до равновесното положение.
Всеки атом има три вибрационни степени на свобода, следователно, в съответствие със закона за равноразпределение, моларният топлинен капацитет на твърдо вещество може да се изчисли като 3nR, като n е броят на атомите в една молекула.
На практика това число е границата, към която се стреми топлинният капацитет на твърдо тяло при високи температури.
Максимум може да се получи при обикновени температури за някои елементи, включително метали. За n=1 законът на Дюлонг и Пети е изпълнен, но за сложни вещества е доста трудно да се достигне до такава граница. Тъй като границата не може да бъде получена в действителност, настъпва разлагане или топене на твърдото вещество.
История на квантовата теория
Основатели на квантовата теория са Айнщайн и Дебай в началото на двадесети век. Тя се основава на квантуването на осцилаторните движения на атомите в определенкристал. В случай на нискотемпературни показатели, топлинният капацитет на твърдо тяло се оказва право пропорционален на абсолютната стойност, взета в кубчета. Тази връзка е наречена закон на Дебай. Като критерий, който позволява да се разграничат индикаторите за ниска и висока температура, е взето сравнението им с температурата на Дебай.
Тази стойност се определя от спектъра на вибрациите на атома в тялото, следователно тя сериозно зависи от характеристиките на неговата кристална структура.
QD е стойност, която има няколкостотин K, но например е много по-висока в диаманта.
Електроните на проводимост имат значителен принос за топлинния капацитет на металите. За изчисляването му се използва квантовата статистика на Ферми. Електронната проводимост за металните атоми е право пропорционална на абсолютната температура. Тъй като това е незначителна стойност, тя се взема предвид само при температури, клонящи към абсолютна нула.
Методи за определяне на топлинния капацитет
Основният експериментален метод е калориметрията. За извършване на теоретично изчисление на топлинния капацитет се използва статистическа термодинамика. Тя е валидна за идеален газ, както и за кристални тела, се извършва въз основа на експериментални данни за структурата на материята.
Емпиричните методи за изчисляване на топлинния капацитет на идеален газ се основават на идеята за химическата структура, приноса на отделни групи атоми към Ср.
За течности се използват и методи, които се основават на използването на термодинамичницикли, които правят възможно преминаването от топлинния капацитет на идеален газ към течност през производната на температурата на енталпията на процеса на изпаряване.
В случай на разтвор, изчисляването на топлинния капацитет като адитивна функция не е позволено, тъй като излишната стойност на топлинния капацитет на разтвора е основно значителна.
За да го оценим, се нуждаем от молекулярно-статистическата теория на разтворите. Най-трудно е идентифицирането на топлинния капацитет на хетерогенните системи в термодинамичния анализ.

Заключение
Изследването на топлинния капацитет ви позволява да изчислите енергийния баланс на процесите, протичащи в химически реактори, както и в други апарати за производство на химикали. В допълнение, тази стойност е необходима за избора на оптимални видове охлаждащи течности.
В момента експерименталното определяне на топлинния капацитет на веществата за различни температурни интервали - от ниски стойности до високи стойности - е основната възможност за определяне на термодинамичните характеристики на веществото. При изчисляване на ентропията и енталпията на веществото се използват интеграли на топлинния капацитет. Информацията за топлинния капацитет на химичните реагенти в определен температурен диапазон ви позволява да изчислите топлинния ефект на процеса. Информацията за топлинния капацитет на разтворите дава възможност да се изчислят техните термодинамични параметри при всякакви температурни стойности в рамките на анализирания интервал.
Например, течност се характеризира с изразходването на част от топлината за промяна на стойността на потенциалната енергияреагиращи молекули. Тази стойност се нарича "конфигурационен" топлинен капацитет, използван за описание на решенията.
Трудно е да се правят пълноценни математически изчисления, без да се вземат предвид термодинамичните характеристики на веществото, неговото агрегатно състояние. Ето защо за течности, газове, твърди вещества се използва такава характеристика като специфичен топлинен капацитет, която позволява да се характеризират енергийните параметри на веществото.






