Идеален газ, уравнението на състоянието на идеалния газ, неговата температура и налягане, обем… списъкът с параметри и дефиниции, използвани в съответния раздел на физиката, може да бъде продължен доста дълго време. Днес ще говорим само по тази тема.
Какво се разглежда в молекулярната физика?

Основният обект, разглеждан в този раздел, е идеалният газ. Уравнението на състоянието на идеалния газ е получено, като се вземат предвид нормалните условия на околната среда и ще говорим за това малко по-късно. Сега нека подходим към този „проблем“отдалеч.
Да кажем, че имаме някаква маса газ. Неговото състояние може да се определи с помощта на три параметъра от термодинамичен характер. Това, разбира се, са налягане, обем и температура. Уравнението на състоянието на системата в този случай ще бъде формулата за връзката между съответните параметри. Изглежда така: F (p, V, T)=0.
Тук, за първи път, бавно се приближаваме до появата на такова нещо като идеалгаз. Нарича се газ, в който взаимодействията между молекулите са незначителни. По принцип това не съществува в природата. Въпреки това, всеки силно разреден газ е близо до него. Азотът, кислородът и въздухът, които са при нормални условия, се различават малко от идеалните. За да напишем уравнението на състоянието за идеален газ, можем да използваме единния газов закон. Получаваме: pV/T=const.
Свързана концепция 1: Законът на Авогадро
Той може да ни каже, че ако вземем еднакъв брой молове от абсолютно произволен газ и ги поставим в същите условия, включително температура и налягане, тогава газовете ще заемат същия обем. По-специално, експериментът е проведен при нормални условия. Това означава, че температурата е била 273,15 Келвина, налягането е една атмосфера (760 милиметра живак или 101325 паскала). С тези параметри газът заема обем, равен на 22,4 литра. Следователно можем да кажем, че за един мол от всеки газ съотношението на числените параметри ще бъде постоянна стойност. Ето защо беше решено тази цифра да се обозначи с буквата R и да се нарече универсална газова константа. По този начин се равнява на 8,31. Единицата е J/molK.
Идеален газ. Идеалното газово уравнение на състоянието и неговата манипулация
Нека се опитаме да пренапишем формулата. За да направите това, ние го записваме в тази форма: pV=RT. След това извършваме просто действие, умножаваме двете страни на уравнението с произволен брой молове. Получаваме pVu=uRT. Нека вземем предвид факта, че произведението на моларния обем иколичеството материя е просто обемът. Но в края на краищата броят на моловете ще бъде едновременно равен на частното от масата и моларната маса. Точно така изглежда уравнението на Менделеев-Клапейрон. Той дава ясна представа за това каква система образува идеалният газ. Уравнението на състоянието за идеален газ ще приеме формата: pV=mRT/M.
Изведете формулата за налягане
Нека направим още няколко манипулации с получените изрази. За да направите това, дясната страна на уравнението на Менделеев-Клапейрон се умножава и разделя на числото на Авогадро. Сега внимателно разглеждаме произведението на количеството вещество по числото на Авогадро. Това не е нищо друго освен общият брой молекули в газа. Но в същото време съотношението на универсалната газова константа към числото на Авогадро ще бъде равно на константата на Болцман. Следователно формулите за налягането могат да бъдат записани, както следва: p=NkT/V или p=nkT. Тук символът n е концентрацията на частиците.
Идеални газови процеси
В молекулярната физика има такова нещо като изопроцеси. Това са термодинамични процеси, които протичат в системата при един от постоянните параметри. В този случай масата на веществото също трябва да остане постоянна. Нека ги разгледаме по-конкретно. И така, законите на идеалния газ.
Налягането остава постоянно
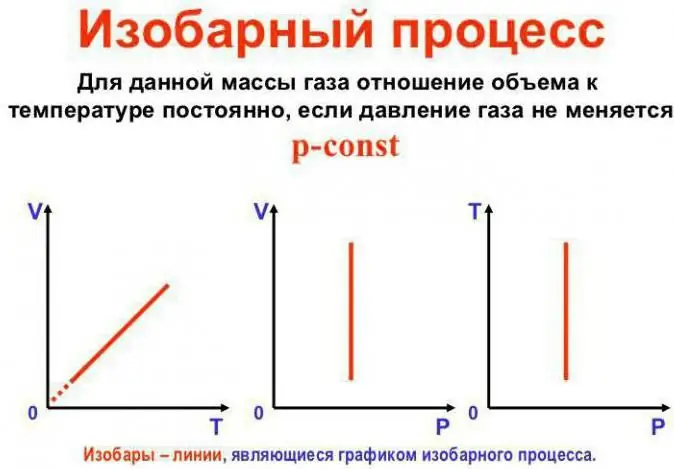
Това е законът на Гей-Люсак. Изглежда така: V/T=const. Може да се пренапише по друг начин: V=Vo (1 + at). Тук a е равно на 1/273,15 K^-1 и се нарича "коефициент на обемно разширение". Можем да заменим температурата както в Целзий, така и вскалата на Келвин. В последния случай получаваме формулата V=Voat.
Обемът остава постоянен

Това е вторият закон на Гей-Люсак, по-често наричан закон на Чарлз. Изглежда така: p/T=const. Има и друга формулировка: p=po (1 + at). Трансформациите могат да бъдат извършени в съответствие с предишния пример. Както можете да видите, законите за идеалния газ понякога са доста сходни един с друг.
Температурата остава постоянна

Ако температурата на идеалния газ остане постоянна, тогава можем да получим закона на Бойл-Мариот. Може да се запише така: pV=const.
Свързана концепция 2: Частично налягане
Да кажем, че имаме съд с газове. Ще бъде смес. Системата е в състояние на топлинно равновесие, а самите газове не реагират един с друг. Тук N ще означава общия брой на молекулите. N1, N2 и така нататък, съответно, броят на молекулите във всеки от компонентите на сместа. Да вземем формулата за налягане p=nkT=NkT/V. Може да се отвори за конкретен случай. За двукомпонентна смес формулата ще приеме формата: p=(N1 + N2) kT/V. Но тогава се оказва, че общото налягане ще бъде сумирано от парциалните налягания на всяка смес. Така че ще изглежда като p1 + p2 и така нататък. Това ще бъдат частичните налягания.
За какво е?
Формулата, която получихме, показва, че налягането в системата е от всяка група молекули. Между другото, не зависи отдруги. Далтън се възползва от това, когато формулира закона, наречен по-късно на негово име: в смес, където газовете не реагират химически един с друг, общото налягане ще бъде равно на сумата от парциалните налягания..






