Природните явления и процеси около нас са доста сложни. За тяхното точно физическо описание трябва да се използва тромав математически апарат и да се вземат предвид голям брой значими фактори. За да се избегне този проблем, във физиката се използват някои опростени модели, които значително улесняват математическия анализ на процеса, но практически не влияят на точността на неговото описание. Един от тях е идеалният газов модел. Нека го разгледаме по-подробно в статията.
Концепцията за идеален газ
Идеалният газ е агрегатно състояние на вещество, което се състои от материални точки, които не взаимодействат една с друга. Нека обясним това определение по-подробно.
Първо, ние говорим за материални точки като обекти, които съставляват идеалния газ. Това означава, че неговите молекули и атоми нямат размер, а имат определена маса. Смело еможе да се направи приближение, като се вземе предвид фактът, че във всички реални газове при ниско налягане и високи температури разстоянието между молекулите е много по-голямо от техните линейни размери.
На второ място, молекулите в идеалния газ не трябва да взаимодействат една с друга. В действителност такива взаимодействия винаги съществуват. Така че дори атомите на благородни газове изпитват дипол-диполно привличане. С други думи, са налице взаимодействията на ван дер Ваалс. Въпреки това, в сравнение с кинетичната енергия на въртене и транслационно движение на молекулите, тези взаимодействия са толкова малки, че не засягат свойствата на газовете. Следователно те не могат да се вземат предвид при решаването на практически задачи.
Важно е да се отбележи, че не всички газове, в които плътността е ниска и температурата е висока, могат да се считат за идеални. В допълнение към взаимодействията на ван дер Ваалс, има и други, по-силни видове връзки, например водородни връзки между H2O молекули, които водят до грубо нарушение на условията за идеалност на газа. Поради тази причина водната пара не е идеален газ, но въздухът е.
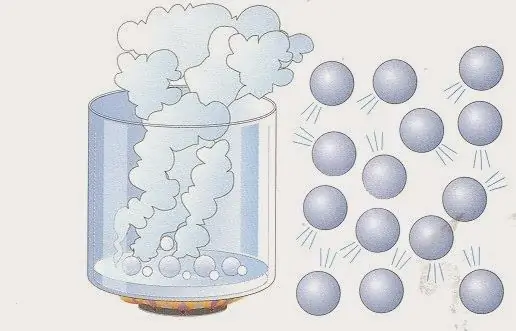
Физически модел на идеален газ
Този модел може да бъде представен по следния начин: да предположим, че газовата система съдържа N частици. Това могат да бъдат атоми и молекули на различни химикали и елементи. Броят на N частиците е голям, така че единицата "мол" обикновено се използва за неговото описание (1 мол съответства на числото на Авогадро). Всички те се движат в някакъв обем V. Движения на частициса хаотични и независими един от друг. Всеки от тях има определена скорост v и се движи по прав път.
Теоретично, вероятността от сблъсък между частиците е почти нула, тъй като размерът им е малък в сравнение с разстоянията между частиците. Ако обаче се случи такъв сблъсък, тогава той е абсолютно еластичен. В последния случай общият импулс на частиците и тяхната кинетична енергия се запазват.
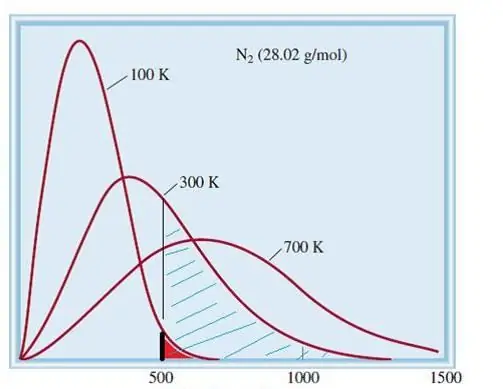
Разглежданият модел на идеални газове е класическа система с огромен брой елементи. Следователно скоростта и енергията на частиците в него се подчиняват на статистическото разпределение на Максуел-Болцман. Някои частици имат ниски скорости, докато други имат високи скорости. В този случай има определена тясна граница на скоростта, в която се намират най-вероятните стойности на това количество. Разпределението на скоростта на азотните молекули е показано схематично по-долу.
Кинетична теория на газовете
Моделът на идеалните газове, описан по-горе, уникално определя свойствата на газовете. Този модел е предложен за първи път от Даниел Бернули през 1738 г.

Впоследствие той е разработен до сегашното си състояние от Август Крьониг, Рудолф Клаузиус, Михаил Ломоносов, Джеймс Максуел, Лудвиг Болцман, Мариан Смолуховски и други учени.
Кинетичната теория на течните вещества, въз основа на която се изгражда моделът на идеалния газ, обяснява две важни макроскопични свойства на системата въз основа на нейното микроскопично поведение:
- Налягането в газовете е резултат от сблъсъка на частици със стените на съда.
- Температурата в системата е резултат от проявлението на постоянно движение на молекули и атоми.
Нека разширим и двете заключения на кинетичната теория.
Налягане на газа
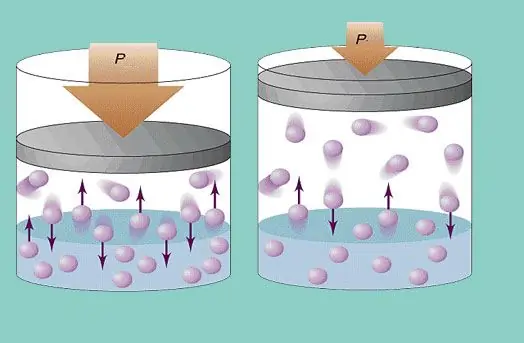
Моделът на идеалния газ предполага постоянно хаотично движение на частици в системата и постоянното им сблъскване със стените на съда. Всеки такъв сблъсък се счита за абсолютно еластичен. Масата на частиците е малка (≈10-27-10-25 kg). Следователно не може да създаде много натиск при сблъсък. Въпреки това броят на частиците, а оттам и на сблъсъците, е огромен (≈1023). В допълнение, средната квадратна скорост на елементите е няколкостотин метра в секунда при стайна температура. Всичко това води до създаване на осезаем натиск върху стените на съда. Може да се изчисли по следната формула:
P=Nmvcp2 / (3V), където vcp е средната квадратична скорост, m е масата на частиците.
Абсолютна температура
Според модела на идеалния газ, температурата се определя уникално от средната кинетична енергия на молекула или атом в изследваната система. Можете да напишете следния израз, който свързва кинетичната енергия и абсолютната температура за идеален газ:
mvcp2 / 2=3 / 2kB T.
Тук kB е константата на Болцман. От това равенство получаваме:
T=m vcp2 / (3kB).
Универсално уравнение на състоянието
Ако комбинираме горните изрази за абсолютно налягане P и абсолютна температура T, можем да напишем следното равенство:
PV=nRT.
Тук n е количеството вещество в молове, R е газовата константа, въведена от Д. И. Менделеев. Този израз е най-важното уравнение в теорията на идеалните газове, тъй като комбинира три термодинамични параметъра (V, P, T) и не зависи от химичните характеристики на газовата система.

Универсалното уравнение за първи път е изведено експериментално от френския физик Емил Клапейрон през 19 век и след това доведено до съвременната си форма от руския химик Менделеев, поради което в момента то носи имената на тези учени.






